生体応答とは?
細胞が分裂・分化や代謝などあらゆる活動を行いますが、それらはいつも全力で行っているわけではなく、必要に応じて行われます。例えば栄養源が乏 しいのに代謝酵素をたくさん合成してしまっているならば、使わないタンパク質を無駄に作ってしまっているといえ、ただでさえ栄養が少ないのに余計なも のを合成すると資源が枯渇してしまいます。また、細胞分裂が再現なく行われてしまったら、多細胞から構成されている生体はバランスを保てなくなってし まいます。
それでは、これらの調節をどのように行っているのでしょうか。細胞は細胞膜を介して外と中を仕切り、細胞の中は一つの閉じた世界となっています。 細胞のあらゆる活動の基となる情報は核内にあるゲノムDNA上に遺伝情報として書き込まれています。例えば細胞分裂ではたらくあるタンパク質Aは、細 胞分裂していないときは細胞内にほとんど存在していません。細胞分裂になるとタンパク質Aを作るためにゲノムDNA上の遺伝子Aが転写→翻訳されま す。では、そもそもタンパク質Aを作るという指令はどこから来るのでしょうか。
細胞は閉じた世界ですが、細胞膜の上には細胞外からの情報を受け取る受容体(レセプター)と呼ばれるタンパク質がたくさん存在しています。例え ば、皮膚が怪我して傷ができてしまったとき、細胞分裂を促す分子(リガンド)が放出され、細胞分裂を促すための受容体に結合します。すると受容体が構 造変化を起こし、細胞内に分裂を促すための信号(シグナル)を送るようになります。このシグナルは細胞内の複数種類のタンパク質を通じて、さながらリ レーのように核まで伝わります。核にはいったシグナルはタンパク質Aを作るべくゲノムDNA上の遺伝子Aの転写を促します。
このような細胞外から細胞内に刺激が伝達することを細胞内シグナル伝達と呼び、それによる適切な応答を生体応答と呼んでいます。細胞分裂だけでな く、代謝や老化、ストレスへの抵抗それぞれで異なる細胞内シグナル伝達経路が働き、適切な生体応答が行われています。
研究内容
当研究室では、線虫および哺乳動物培養細胞を用いて、大きく分けて以下の2つのテーマで研究を進めています。
老化制御・ストレス応答に関する研究
I) 老化に関する研究生物は成長し、老いていくことは基本的には避けられません。その過程でどのような生体応答が起きているのかは多くの人が興味を持つところであり、さかん に研究が行われています。しかしながら老化のメカニズム等、その全体像が明らかになったとはいえません。当研究室では主にモデル動物として線虫(C. elegans)を用い、老化の制御に関与する生体応答を行っている遺伝した、それらを活性化させる生理活性物質の探索と同定、また、それら がどのようなしくみで作用するかについて解析を行っています。
当研究室は、老化の中でも特に健康寿命について関心を持っています。健康寿命とは、「支障なく生活が行える期間」のことです。全寿命のうち、この健康寿 命の期間が長いほど年を取っても元気でいられることをあらわしており、生活の質(QOL)も高いといえます。日本の平均寿命は世界一で、現在も延び続けて います。しかしながら
健康寿命と寿命のあいだには10年程度の差があるため、健康寿命を延ばすことが超高齢化社会を迎えている日本において求められています。
健康寿命を阻害するのは「メタボリックシンドローム(代謝症候群)」や「ロコモティブシンドローム(運動器症候群)」です。これらは老化に伴い発生しや すくなり、前者により代謝の低下と脂肪(特に内臓脂肪)の蓄積が高血圧、脂質異常症、糖尿病等を引き起こし、心血管系の疾患やさまざまな合併症に至るおそ れがあります。また、後者は加齢による神経や筋肉の機能低下や骨粗鬆症に結びつきます。線虫もヒトと同様、健康寿命を持っており、老化に伴い脂肪の蓄積や 運動能力の低下が生じます。われわれは線虫を用いて健康寿命が損なわれるこの過程で何が起きているのかを遺伝子レベルで解析し、健康寿命を制御する生体応 答のしくみや、それらを活性化させる生理活性物質に注目して研究を進めています。
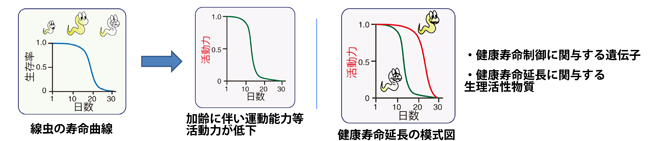
i)細胞外マトリクス(ECM)リモデリングと老化に関する研究
生物は細胞から構成されていますが、決して細胞のみの集合体でなく、細胞から分泌された細胞外マトリクス(ECM)が体の構造に極めて重要な役割を果た しています。ECMはコラーゲン、フィブロネクチン、ラミニン、プロテオグリカンなどのタンパク質等から構成されており、組織 の構造を維持するだけでなく、細胞の足場としての機能や情報伝達の場としても利用されます。このECMは一度作られたら半永久的に維持されるわけではな く、形成と破壊を繰り返すリモデリングというバランスの上に成り立っています。
加齢に伴いリモデリングの能力が低下したり、ECMタンパク質が損傷を受けるとECMとしての機能も低下します。例えば真皮の老化に伴うECMの機能低 下はしわやたるみを引き起こします。ECMの機能低下は紫外線(UV)や活性酸素など内外のストレスによっても発生します。このため、ECMの機能維持は 老化の進行を抑えるのに有効であると期待されます。しかしながらECMの機能を維持する仕組みは十分にわかっていません。
コラーゲンを酸分解して得たコラーゲントリペプチド(CTP)は、コラーゲン産生を増加させる作用を持つことが知られていましたが、どのような仕組みで それが調節されているか明らかではありませんでした。当研究室で線虫を用いた解析により、CTPがp38 MAPキナーゼカスケードを活性化させ、転写因子SKN-1を介してコラーゲン遺伝子の発現を増加させるだけでなく、老化の進行にブレーキをかけ、寿命を 延長する作用があることを見出しました。
II) ストレス応答に関する研究
われわれは酸素なしでは生きてはいけませんが、その酸素は基本的に呼吸で用いられます。しかしながら一部の酸素は細胞内(ミトコンドリア)で利用される 過程で不安定な活性酸素種(ROS: Reactive Oxygen Species)へと変化します。酸素はものが燃えるのを助けるはたらきがあり、酸素が結合したものは酸化されます。ROSはふつうの酸素O2よりもきわめて反応性が高 く、産生されたROSは手当たり次第に近くの物質を酸化してしまいます。これが細胞内で発生すると、核酸やタンパク質など細胞内の重要な分子を酸化してし まい、細胞にダメージを与えてしまいます。これを酸化ストレスといいます。呼吸の過程で用いられる酸素だけでなく、紫外線や電磁波、有害な化合物が細胞内 でROSを発生させ、酸化ストレスとなります。もちろん細胞はROSが発生するとそれを察知し、ROSを無害化するような応答を行い、酸化ストレスを軽減 させるための仕組みを持っています。老化にもROSが関与すると考えられており、ROSを除去する物質を与えた線虫は寿命が延びると考えられています。当 研究室では老化との関連から、ストレス応答についても研究を進めています。

線虫を用いて得られた結果は、線虫のみならずヒトにおいてもあてはまるかを、ヒト正常細胞や細胞株等を用いて調べ、種を超えて保存された機構を明らかに します。
がんに関する研究
われわれの研究室では、がんの細胞生物学についての研究も行っています。がんは、がん遺伝子またはがん抑制遺伝子と呼ばれる遺伝子の異常によって起こり ますが、これらの遺伝子は元々細胞の増殖や生存を制御するための生体応答因子として働いているものです。がん遺伝子はがん細胞でしかみられないのではな く、正常な細胞でも存在し、例えば細胞の増殖を促進させるような働きをしています。ヒトの体の中には2つで一組の遺伝子が存在していますが、がん遺伝子が 異常になると例え2つのうち一つの遺伝子に異常が生じた場合でも細胞の増殖が異常に促進されることになり、がん化しやすくなります。一方、がん抑制遺伝子 は基本的にはがんを「抑える」はたらきをしている遺伝子なので、片方の遺伝子異常だけ(もう片方は正常)ではがんの抑制効果があります。このことから、ど のような遺伝子ががんに関与しているかを調べるうえで、がん遺伝子は現象が顕著であるためわかりやすいもののがん抑制遺伝子は解析がやや難しく、研究が遅 れていました。近年、遺伝子異常の系統をつくりやすいモデル生物を用いた研究により、新しいがん抑制遺伝子が次々と発見・同定され、極めて重要な生体応答 経路の存在が明るみとなりました。そのHippo経路とよばれる生体応答経路は、もとはショウジョウバエの器官形成異常(巨大化、不定形化)をもたらす変 異体から同定され、組織や器官のサイズを適切に調節する応答経路ということがわかりました。さらに多くの研究の結果、Hippo経路は生物間で広く保存さ れており、多様な働きを担っていることがわかりました。例えば組織や器官のサイズの制御、上皮細胞の極性、幹細胞の維持など、生命にとって必要不可欠な箇 所ではたらいています。下の図に示すようにHippo経路は様々な因子によって構成されており、細胞同士の接着などを起点として、細胞分裂の調節やアポ トーシスの制御によって上記の役割を果たしているとされています。Hippo経路は比較的最近発見されたものなので、その応答経路の全体像や生体内での役 割などの全容がわかったとはいえません。われわれは立命館大学生命科学部生命医科学科、病態細胞生物学研究室と共同研究により、この経路の制御に関与する 新規因子とその役割について研究を行っています。
Hippo経路は細胞接触などをきっかけとしてMST1/2→LATS1/2→YAPへとシグナルが伝わります。YAP はこのシグナルがないと細胞核に入ってしまいますが、シグナルによって細胞質へと所在が変わります。このYAPの細胞内での所在をコントロールすることによりHippo経 路は細胞増殖やアポトーシスをコントロールしています。
われわれは、Hippo経路と相互作用する新規因子をスクリーニングで単離、同定するとともにその機能について解析を行っています。TRIM3はわれわ れが同定したHippo経路の制御に関与すると考えられるTRIM/RBCC E3ユビキチンリガーゼの一つで、基質となるタンパク質のユビキチン化などに関与します。ユビキチン化はタンパク質の分解だけでなく細胞内での所在や活性にも関与すること が報告されているため、TRIM3がHippo経路の活性に影響を与えていると考え、研究を進めています。
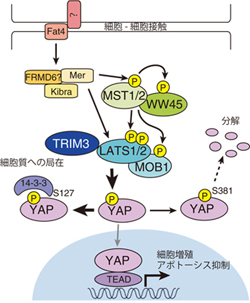
図. Hippo経路とTRIM3